Хр миелолейкоз молекулярный пцр закл крови расшифровка. Хронический миелоидный лейкоз - клиника, диагностика, лечение
Хронический миелолейкоз – заболевание крови опухолевого генеза, в основе которого лежит хромосомная перестройка с образованием химерного гена и усиленная пролиферация клеток-предшественников миелопоэза. В 95 % случаев у больных выявляется постоянная приобретенная хромосомная аномалия – так называемая филадельфийская хромосома (транслокация, то есть перемещение генетического материала дистальных (конечных) отделов длинных плеч 9 и 22 хромосомы).
Заболевание регистрируется во всем мире с примерно одинаковой частотой. Ежегодно выявляется 1 новый случай болезни на 100 тысяч населения. В структуре лейкозов на долю данной патологии приходится около 20 %. Хронический миелолейкоз встречается во всех возрастных группах, реже – у лиц моложе 20 лет. Пик заболеваемости приходится на 40-50 лет. Мужчины болеют несколько чаще, чем женщины.
Клинические проявления
У 9 из 10 больных хроническим миелолейкозом в кариотипе обнаруживается филадельфийская хромосома - транслокация длиных плеч дистальных отделов 9 и 22 хромосом.У многих больных хронический миелолейкоз начинается исподволь. Нередко такой диагноз выставляется по анализу крови на фоне полного благополучия.
В клинической практике принято выделять 2 основные стадии болезни:
- Развернутая.
- Терминальная (с бластными кризами).
Развернутая стадия заболевания характеризуется моноклональностью (одинаковостью) клеток миелоидного ряда. При этом элементы нормального кроветворения практически вытеснены. В костном мозге выявляется большой процент клеток с филадельфийской хромосомой. Реже встречаются варианты заболевания с длительно сохраняющимся нормальным кроветворением.
На ранних этапах развития болезнь имеет либо бессимптомное, либо малосимптомное течение. Таких пациентов может беспокоить:
- немотивированная общая слабость;
- быстрая усталость и снижение работоспособности;
- отсутствие аппетита;
- повышенная потливость;
- тяжесть и болевые ощущения в левом подреберье (особенно после быстрой ходьбы или приема пищи).
У них увеличивается селезенка и печень, нарастают изменения в крови и костном мозге. Причем первые проявления болезни нередко связаны именно с большими размерами селезенки. Лимфатические узлы на начальных стадиях болезни обычно не поражаются.
При данной патологии страдает также фагоцитарное звено иммунитета. Это является причиной повышенной склонности к инфекционным заболеваниям и осложнениям.
Астенический синдром обусловлен повышенным клеточным распадом и особенностями продукции гранулоцитов, составляющих основную массу лейкоцитов.
При очень высоком уровне лейкоцитов (500×10⁹/л и более) в связи с их скоплением в сосудах и стазом крови возможно нарушение кровообращения в тканях (особенно в головном мозге) и .
Постепенно патологический процесс прогрессирует. В крови появляются анеуплоидные клетки с неправильным хромосомным набором, которые образуют новые субклоны опухолевых клеток, не способные к дифференцировке, то есть к образованию нормальных лейкоцитов, но быстро пролиферирующие (делящиеся) и подавляющие исходные дифференцирующиеся клетки. В этот период болезнь переходит в терминальную стадию. Самочувствие пациентов продолжает ухудшаться. Снижается эффективность ранее проводимого лечения. Клинически это проявляется:
- быстрым ;
- лихорадкой с ознобами и проливными потами;
- сильными болями в костях;
- формированием очагов опухоли в лимфатических узлах;
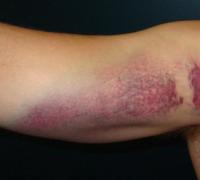
- образованием лейкемидов на коже (представляют собой скопления опухолевых клеток; имеют вид пятен розоватого или коричневатого цвета);
- выраженной слабостью;
- истощением.
Течение болезни может быть различным. У одних больных оно относительно доброкачественное и лейкозный процесс развивается много лет. У других оно агрессивное с быстрым прогрессированием, приводящее в течение нескольких месяцев к гибели больного.
Изменения в крови
Первым признаком лейкоза могут быть изменения в . У многих больных они появляются задолго до клинической манифестации болезни.
В развернутой стадии картина крови характеризуется:
- увеличением общего числа лейкоцитов (от 20 до 200×10⁹/л, а иногда и более);
- сдвигом в формуле крови до юных форм (промиелоцитов и метамиелоцитов);
- наличием единичных бластных клеток;
- увеличением процентного содержания базофилов и эозинофилов;
- ускорением СОЭ.
Количество тромбоцитов может оставаться нормальным или несколько снижаться. Однако в ряде случаев с самого начала болезни выявляется высокий тромбоцитоз (1500-2000×10⁹/л).
Красная кровь на ранних этапах патологического процесса существенно не меняется. Но у части больных уже в этот период появляется .
Морфологически клетки крови практически не отличаются от таковых в норме. Однако некоторые особенности имеют гранулоциты:
- скудная зернистость;
- уменьшение содержания миелопероксидазы в миелоцитах, метамиелоцитах, нейтрофилах;
- снижение (иногда до нуля) щелочной фосфатазы в зрелых нейтрофилах.
По мере прогрессирования и накопления опухолевых клеток увеличивается лейкоцитоз и ухудшается состояние больных. Вскоре болезнь переходит в терминальную стадию и показатели анализа крови еще больше усугубляются. При этом наблюдается:
- анемия (рефрактерная к лечению);
- увеличение концентрации миелоцитов, промиелоцитов, бластов.
Характерным признаком болезни в терминальной стадии является бластный криз. Это состояние, при котором в крови и костном мозге растет содержание бластных клеток больше 20 %. Морфология клеток при бластном кризе отличается большим разнообразием. Они являются потомками колониеобразующих клеток, поэтому нередко имеют четкие признаки родоначальников того или иного клеточного ряда. Они могут быть:
- недифференцированные;
- миелобластные;
- лимфобластные;
- миеломонобластные;
- монобластные;
- эритробластные;
- мегакариобластные.
В связи с нарушением костномозговых барьеров в крови обнаруживаются осколки ядер мегакариоцитов и большое количество эритрокариоцитов.
В конечном итоге нормальное кроветворение полностью угнетается. Патологический процесс выходит за пределы костного мозга. Бластные клетки метастазируют в различные органы и ткани.
Постановка диагноза
 Золотой стандарт диагностики - биопсия костного мозга с последующим исследованием его клеточного состава.
Золотой стандарт диагностики - биопсия костного мозга с последующим исследованием его клеточного состава. Заподозрить наличие у больного хронического миелолейкоза врач может по характерным изменениям анализа крови и клиническим проявлениям. Особенно следует обратить внимание на немотивированный нейтрофильный лейкоцитоз с разной степенью омоложения лейкоцитарной формулы в сочетании с увеличением селезенки.
Для подтверждения диагноза должна проводиться трепанобиопсия костного мозга с исследованием его клеточного состава.
В развернутой стадии хронического миелолейкоза костный мозг богат клеточными элементами.
- В клеточном составе преобладают клетки гранулоцитарного ряда. Их соотношение с эритроцитами достигает 20:1 в пользу гранулоцитов.
- Процентное содержание бластов превышает 10 %.
- Может регистрироваться увеличенное количество мегакариоцитов с чертами дисплазии и избыточное выпадение ретикулиновых волокон.
- В терминальной стадии в костном мозге увеличивается число бластных клеток и соответственно снижается количество переходных форм и зрелых элементов.
В классических случаях трудностей с постановкой диагноза не возникает. Но они могут появляться при нерезко выраженных клинико-лабораторных изменениях. Тогда правильно поставить диагноз помогает цитогенетическое и молекулярно-генетическое исследование. Они позволяют выявить филадельфийскую хромосому и другие хромосомные поломки.
Дифференциальная диагностика проводится:
- с лейкемоидными реакциями (в ответ на инфекцию, опухоль);
- эссенциальной тромбоцитопенией;
- хроническим миеломоноцитарным лейкозом и т. д.
Общие принципы лечения
Лечение хронического миелолейкоза неоднозначно и зависит от стадии болезни, тяжести ее течения. Оно направлено:
- на уменьшение опухолевой массы;
- нормализацию состава крови;
- повышение качества жизни больных;
- увеличение ее продолжительности.
Основными методами лечения являются:
- химиотерапия;
- трансплантация костного мозга.
В настоящее время для химиотерапии используются:
- гидроксимочевина (применялась для лечения хронического миелолейкоза больше половины столетия; с ее помощью удавалось снизить количество опухолевой массы и добиться нестойкой ремиссии);
- препараты α-интерферона (считаются более эффективными, но имеют много побочных явлений);
- ингибиторы тирозинкиназы (хорошо переносятся больными, вызывают мало побочных эффектов; угнетают пролиферацию опухолевых клеток, практически не влияя на здоровые аналоги; однако эффективны не у всех больных, что связано с развитием резистентности).
Алогенная трансплантация костного мозга является единственным методом, позволяющим излечить больного. Но риск осложнений после нее остается высоким и составляет около 20-40 %.
Миелолейкозом называют злокачественное перерождение стволовых клеток костного мозга, который отвечает за производство форменных элементов крови-красных и белых кровяных телец и тромбоцитов. При миелолейкозе (белокровии, ) костный мозг производит бластные, недозревшие клетки, которые, постепенно, вытесняют из кровяного русла нормальные форменные элементы.
Заболевание носит преимущественно хронический характер и поражает в основном, взрослых. Для постановки диагноза необходимо провести анализ крови на миелолейкоз. Поскольку на разных стадиях заболевания, происходят значительные изменения в , требуется проводить анализы несколько раз. При подозрении на миелолейкоз, врачи рекомендуют проводить регулярные обследования.
Причины
Миелолейкоз - это результат мутирования в костном мозге. Аномальная клетка теряет способность нормально функционировать и начинает стихийно делиться. Раковые клетки, размножаясь, постепенно вытесняют здоровые. В результате возникают и анемии и организм теряет защиту от инфекций. Лейкозные клетки проникают в лимфоузлы, кооперируются в опухоли и провоцируют патологические процессы.
Причиной миеломной болезни может стать радиоактивное излучение или воздействие канцерогенов, среди которых имеются лекарственные препараты, растворители краски средства борьбы с грызунами и насекомыми.
Наследственные факторы при лейкозе, как и при других болезнях, имеют место. В семьях, где родственники заболевают миеломной болезнью, велика вероятность заболеваний среди потомков. Детям передаётся не сама болезнь, а предрасположенность к ней.
Существует гипотеза о инфекционной этиологии заболевания. В этом случае, имеет значение раса и место проживания человека.
Диагностика
Предварительный диагноз на миелолейкоз ставится на основании результатов , стандартной диагностической процедуры при любом заболевании. Врача должно насторожить увеличение числа лейкоцитов.
На миеломную болезнь, прежде всего, должна учитывать количество лейкоцитов и их соотношение с расчётом лейкоцитарной формулы. При подсчёте лейкоцитарной формулы наблюдается сдвиг влево, появление промиелоцитов. Растёт процент базофилов и эозинофилов, . Число тромбоцитов в норме, или несколько повышено. Наблюдаются симптомы анемии в лёгкой форме.
Если миелолейкоз прогрессирует, меняются. Поэтому, необходимо повторять анализ крови на миелолейкоз через некоторое время. Результаты исследований выявляют сильную анемию, форменные элементы меняют размеры и деформируются, (анизоцитоз и пойкилоцитоз);число лейкоцитов многократно увеличивается в сравнении с прежними результатами. Количество бластных клеток достигает 15%. и эрзинофилов превышает норму. Блокируется действие щелочной фосфатазы в нейтрофилах.
Сопутствующими миелолейкозу симптомами являются проблемы с печенью, подтверждающиеся повышением активности сывороточных энзимов –аланинаминотрансферазы и щелочной фсфатазы.
Симптомы
Симптомы миелолейкоза являются:
- Боли в костях. Болят бедренные кости, позвоночник, таз, рёбра;

- Патологические переломы;
- Гиперкальциемия. Проявляется рвотой, тошнотой, запорами, полиурией. Могут возникнуть мозговые нарушения, человек впадает в летаргию или кому;
- Заболевания почек. Нефропатия проявляется в виде повышения содержания кальция и мочевой кислоты в крови, появления белка в моче;
- Анемия нормохромная. в норме, резко вырастает СОЭ;
- Остеопороз;
- Сдавливание спинного мозга опухолями позвоночника. Проявляется в виде болей в спине, усиливающихся при кашле, чихании. Нарушается работа мочевого пузыря и кишок.;
- Беззащитность перед бактериальными инфекциями. Связана с ослаблением иммунитета;
- Геморрагии. , матки, дёсен, подкожные кровоизлияния.
Подготовка к анализу
Правила сдачи крови на общий анализ не предусматривают специфических правил подготовки. Как сдавать анализ крови на хронический миелолейкоз, известно. , утром, чтобы избежать «помех», искажающих результаты. В день, перед сдачей крови не рекомендуют тяжёлые физические нагрузки. Крайне нежелательно, в течение трёх суток перед процедурой, употребление жирных и жареных продуктов. Если эти условия соблюдены, то диагностический анализ крови на миелолейкоз будет чрезвычайно информативен.
Делают или пальца. Венозная кровь более концентрирована, чем капиллярная, поэтому некоторые врачи требуют именно такого отбора проб на анализ.
Расшифровка результатов миелолейкоза, занимает два дня, с момента принятия результатов в обработку. Если лаборатория перегружена работой, то результат может быть получен позднее.
Предусматривают взятие образцов костного мозга на цитогенетический анализ из бедренной кости. Пробы отбирают методом биопсии или аспирации. Изучают хромосомы. Поражённые клетки содержат аномальную 22 хромосому. С целью обнаружения аномальной хромосомы используют цепную полимеразную реакцию.
Лечение
Качество анализа является залогом успешной терапии. Выбор метода лечения и интенсивность рекомендуемых процедур зависят от фазы заболевания. У части больных миеломной болезнью наблюдают нарастающее прогрессирование процесса на протяжении многих лет, и не требующие противоопухолевого лечения.
У больных при наличии метастазов применяют локальную лучевую терапию. При медленном развитии миелолейкоза используют выжидательную тактику.

Если нарастают боли, что свидетельствует о разрастании опухоли, назначают цитостатики. Сроки лечения, при условии наличия позитивных результатов продолжаются до двух лет.
Проводят лечение, профилактирующие осложнения. Для купирования гиперкальциемии применяют кортикостероиды на фоне обильного питья. Применяют лекарства для лечения заболеваний почек и остеопороза.
Прогноз
Миеломное заболевание в вялотекущей фазе не является показанием для немедленного лечения. Необходимостью для начала терапии является появление в крови парапротеина, или понижение вязкости, наличие кровотечений, болей в костях, переломах, гиперкальциемия, поражение почек, компрессия спинного мозга, инфекционные осложнения.
Сдавливание спинного мозга требует хирургического лечения, а также, местного облучения. Переломы костей требуют ортопедического фиксирования.
В ряде случаев, если не показана радиационная терапия, используют цитотоксическое лечение. В этом случае надо иметь ввиду, что побочным эффектом может стать вторичная миелолейкемия.
При отсутствии лечения больные миеломной болезнью живут до двух лет. Полное излечение миеломы-это дело будущего.
Современные методы лечения способны затормозить разрушительное действие заболевания на организм и бороться с её конкретными симптомами.
Хронический миелолейкоз – болезнь крови опухолевой этиологии. При ее развитии наблюдается бесконтрольный рост и размножение всех ростковых кровяных клеток. Патологические изменения в одной из хромосом вызывают образование мутированного гена, который и становится причиной нарушения кроветворения в красном костном мозге и, как следствие, — усиленного роста клеток.
Международная классификация болезней десятого пересмотра (МКБ 10) присваивает заболеванию код С92. Оно может протекать в 3 формах, что зависит от стадии. С учетом того, насколько своевременно был диагностирован хронический миелолейкоз, определяют максимальную продолжительность жизни больного.
Причины развития
Рост и функционирование здоровых клеток в организме происходит на основе информации, которую содержат хромосомы. Когда конкретная клетка делится, это создает новую копию ДНК в хромосомах. Если такой процесс деления нарушен, могут образовываться мутирующие гены, которые и влияют на развитие онкологических патологий.
В организме человека имеются гены, которые стимулируют процесс развития клеток – онкогены. Также содержатся и гены, которые замедляют их рост, что необходимо для смерти клетки в нужное время – супрессоры. При нарушении деятельности таких генов наблюдается перерождение здоровых клеток в онкологические и выключение из данного процесса супрессоров.
Современная медицина не имеет достаточно конкретных сведений о том, почему развивается хронический миелолейкоз, в том числе и острый. Этот вопрос находится в стадии изучения. Имеются предположения, что на развитие заболевания влияют некоторые предрасполагающие факторы:
- Воздействие на организм радиоактивного облучения . Доказательством этому можно назвать случай с Нагасаки и Хиросимой. История болезни (МКБ 10 – С92) японцев, находящихся в области аварии, гласит, что большинство из них были подвержены развитию хронического миелолейкоза.
- Вирусное поражение организма, а также электромагнитные лучи и химические вещества , воздействующие на организм. Такой фактор, как потенциальная причина развития заболевания, на сегодняшний день еще рассматривается исследователями.
- Наследственная предрасположенность . Люди, страдающие врожденными хромосомными патологиями, находятся в зоне повышенного риска заболеваемости миелоидным лейкозом. В большинстве случаев – это лица, у которых диагностирован синдром Дауна или Клайнфелтера.
- Лечение опухолевидных новообразований определенными медикаментами по типу цитостатиков в комплексе с облучением.
Все такие предрасполагающие факторы вызывают структурное нарушение клеточных хромосом в красном костном мозге и образование новых ДНК с аномальным строением. При этом число последних начинает настолько увеличиваться, что они вытесняют здоровые клетки. В это время наблюдается бесконтрольный рост аномальных клеток по аналогии с раковыми.
Стадии развития заболевания
Большинство людей (около 80%) обращаются в больницу уже во время того, когда заболевание переходит в хроническое течение. В это время наблюдается слегка выраженные симптомы миелолейкоза, которые не редко путают с обычным переутомлением: общее недомогание, снижение трудоспособности, усиленное потоотделение.
Хроническая форма заболевания может протекать бессимптомно на протяжении 2-3 месяцев, а иногда и намного дольше – до нескольких лет. В некоторых случаях миелолейкоз диагностируют совершенно случайно, проводя анализ крови для выявления иной патологии в организме.
Хронический миелолейкоз может сопровождаться осложнениями в форме повышения общей температуры до высоких показателей, болевого синдрома в области левого подреберья и др. При наличии осложнений данная форма заболевания развивается на протяжении 4 лет и более.
Если не начать своевременно лечение заболевания хронической стадии, оно переходит во 2 стадию – акселерацию. Незрелые лейкоциты усиленно вырабатываются, доходя до объема в 10-19%. Данная стадия длится, примерно, в течение года. На данном этапе развития присоединяется иная симптоматика, которая усугубляет общее состояние больного: развивается анемия, происходит увеличение селезенки, а лекарственные препараты, используемые в лечении, не приносят той эффективности, как на начальном этапе развития заболевания.
Если не начать лечение на стадии акселерации, болезнь переходит в терминальную стадию, патогенез которой характеризуется увеличением числа злокачественных клеток в костном мозге и полным отсутствием в нем здоровых клеток. В таком случае исход наименее благоприятен и назначенное врачом лечение, зачастую, оказывается уже неэффективным.
Симптомы
Хронический миелоцитарный лейкоз (ХМЛ) может иметь разную симптоматику, что зависит от того, на какой стадии развивается заболевание. Общими для всех стадий симптомами можно назвать:
- выраженное общее недомогание;
- снижение веса;
- снижение либо полная утрата аппетита (в зависимости от стадии заболевания);
- селезенка и печень при хроническом миелолейкозе увеличиваются;
- побледнение кожных покровов;
- болевой синдром в костях;
- усиление потливости.
Если рассматривать клинику заболевания с учетом его стадии, она выглядит так:
- Хроническая : быстрое насыщение во время приема пищи, болевой синдром в левом подреберье, одышка и чувство нехватки воздуха при физической нагрузке, головная боль, нарушение зрительной функции. У мужчин может возникать длительная болезненная эрекция.
- Стадия акселерации . На данном этапе развивается анемия прогрессирующего течения, общие патологические симптомы усиливаются в своей интенсивности, патологические лейкоцитарные клетки находятся на повышенном уровне содержания в крови.
- Терминальная . Общее состояние больного ухудшается до критических показателей. Возникает лихорадочный синдром, общая температура повышается до максимальной отметки. Также развитие терминального миелоза характеризуется кровотечением через слизистые оболочки, кожные покровы, кишечник. За счет увеличения селезенки и печеночных долей возникает болевой синдром в левом подреберье и чувство тяжести.
Диагностика
На разных стадиях развития заболевания требуется специфическая диагностика. На начальном этапе протекания назначают:
- Проведение общего анализа крови . Исследование помогает выявить незначительное снижение составляющих крови: гемоглобина и эритроцитов. Часто их уровень остается в норме на данной стадии развития болезни. Можно обнаружить наличие умеренного тромбоцитоза, базофилии, эозинофилии. Картина крови при хроническом миелолейкозе показывает лейкоцитоз с показателями 15-30*109/л.
- Проведение биохимического анализа . Диагностика показывает повышение объема содержания мочевой кислоты в организме.
- Проведение стернальной пункции костного вещества . Мегакариоциты превышены в своем уровне содержания, а также гранулоцитарные клетки юных форм.
На стадии акселерации необходимо проведение следующих диагностических мероприятий:

На терминальной стадии выявить патологию можно проведением:
- Общего анализа крови , который помогает обнаружить критическое снижение объема эритроцитов, тромбоцитов и гемоглобина, повышение объема базофилов до 20%. Лейкоцитоз достигает 500-1000*109/л.
- Стернальной пункции , которая помогает выявить критическое увеличение содержания злокачественных клеток в мозговом веществе, а также базофилов и эозинофилов.
- Цитогенетического анализа , который помогает выявить наличие филадельфийской хромосомы в организме.
Как лечить болезнь
Миелоидная болезнь крови требует специфического лечения, тип которого определяют с учетом стадии протекания. В том случае, если клиника заболевания не сильно выражена или же вовсе отсутствует, назначают соблюдение правильного рациона питания, прием витаминных препаратов, проведение общеукрепляющих процедур. В данном случае требуется систематическое наблюдение у лечащего врача.
Если присоединились явно выраженные симптомы, назначают прием лекарственных средств-цитостатиков, блокирующих рост патологических клеток. Несмотря на высокую эффективность препаратов, они способны вызывать побочные явления: тошноту, общее недомогание, выпадение волосяного покрова, воспаление желудка или кишечника.
В тяжелых случаях проводят пересадку костного мозга и переливание крови. Иногда такое лечение помогает навсегда избавить человека от заболевания. Единственное условие – полная совместимость донорского вещества с костным мозгом больного.
Народные средства в лечении хронического лейкоза не будут эффективными. Таковые используют лишь для укрепления иммунитета человека и повышения защитных сил организма. Отличным медикаментозным средством в терапии заболевания считается Гливек, с помощью которого можно вызвать гематологическую ремиссию патологии. Входящие в состав препарата вещества блокируют и уничтожают филадельфийскую хромосому.
В крайне тяжелом случае необходима полная резекция (удаление) селезенки, что позволяет улучшить общее состояние больного и повысить эффективность проводимой терапии.
Хронический миелолейкоз (ХМЛ) - миелопролиферативное хроническое заболевание, при котором наблюдается повышенное образование грануло-цитов (преимущественно нейтрофилов, а также промиелоцитов, миелоци-тов, метамиелоцитов), являющихся субстратом опухоли. В большинстве случаев закономерным исходом болезни является бластный криз, характеризующийся появлением большого количества бластных клеток, рефрак-терностью к терапии и заканчивающийся летально.
Этиология и патогенез. Причиной патологического роста клеток считается мутация клетки-предшественницы миелопоэза (частично детерминированная полипотентная клетка). Это доказывается обнаружением у больных ХМЛ специфического маркера - патологической Ph-хромосомы (филадельфийской) в клетках миелоидного, эритроидного, моноцитарного и тромбоцитарного ростков. Ph-хромосома является частым клеточным маркером, подтверждающим происхождение всего патологического клона клеток при ХМЛ от одной материнской. Несмотря на то что лейкозными являются все три ростка костного мозга, в развернутой стадии ХМЛ наблюдается безграничный рост, как правило, одного ростка - гранулоцитарно-го. Существенно повышается в костном мозге продукция мегакариоцитов, в периферической крови - тромбоцитов.
По мере течения болезни моноклоновая стадия сменяется поликлоно-вой, что доказывается появлением клеток с различным неправильным набором хромосом. В этом проявляется закон опухолевой прогрессии, которому подчиняется данный лейкоз.
ХМЛ чаще наблюдается у взрослых в возрасте 30-70 лет; отмечается небольшое преобладание мужчин. ХМЛ - наиболее распространенный и всех лейкозов, на него приходится 20 % гемобластозов у взрослых лиц-
Классификация. Как отмечалось, заболевание закономерно проходит своем развитии две стадии - моноклоновую и поликлоновую. Этому с°° ветствуют три стадии хронического миелолейкоза в клиническом отоор жении.
Стадия I - начальная - миелоидная пролиферация костного мо га + небольшие изменения в крови без явлений интоксикации (в периф рической крови отмечается до 1-3 % бластов). ^е
Стадия II - развернутая - выраженные клинико-гематологиче ^ проявления (интоксикация продуктами распада лейкозных клеток, увел
Е печени и селезенки, миелоидная пролиферация костного мозга + изме-нИ иЯ в крови). В периферической крови до 10 % бластов. 116 Стадия Ш - терминальная (соответствует развитию поликлоновой пухоли) - рефрактерность к проводимой цитостатической терапии, исто-° ение, значительное увеличение селезенки и печени, дистрофические изменения внутренних органов, выраженные изменения крови (анемия, л омбопитопения). Для терминальной стадии ХМЛ характерно развитие
I называемых бластных кризов - появление в периферической крови йгастных клеток (до 30-90 %), в связи с чем заболевание приобретает чер-ы острого лейкоза. Чаще всего в костном мозге и периферической крови й стный КрИЗ характеризуется появлением миелобластов, однако могут встретиться и недифференцируемые бластные клетки. При кариологиче-ском исследовании выявляется поликлоновость патологических клеток. Одновременно происходит значительное угнетение тромбоцитопоэза, развивается геморрагический синдром. Встречается также лимфобластный вариант бластного криза (в костном мозге и периферической крови появляется большое количество лимфобластов).
Клиническая картина. Клинические проявления ХМЛ могут выражаться большими синдромами.
Миелопролиферативный синдром, в основе которого лежит миелоидная пролиферация костного мозга, включает:
А) общие симптомы, вызванные интоксикацией, разрастаниями лейкоз ных клеток в костном мозге, селезенке и печени (потливость, слабость, снижение массы тела, тяжесть и боль в области селезенки и печени), ос- салгии;
Б) увеличение печени и селезенки;
В) лейкемические инфильтраты в коже;
Г) характерные изменения в костном мозге и периферической крови. Синдром, обусловленный осложнениями:
А) геморрагический диатез (геморрагии и тромбозы вследствие наруше ния прокоагулянтного и тромбоцитарного звеньев гемостаза);
Б) гнойно-воспалительные (пневмонии, плевриты, бронхиты, гнойные поражения кожи и подкожной жировой клетчатки), обусловленные резким снижением активности иммунитета;
В) мочекислый диатез (гиперурикемия вследствие повышенного распада гранулоцитов).
Различная выраженность синдромов на разных стадиях болезни обусловливает достаточно полиморфную клиническую картину. Можно наблюдать больных, не предъявляющих никаких жалоб и вполне трудоспособных, и больных с тяжелыми поражениями внутренних органов, истощенных, полностью потерявших трудоспособность.
На I этапе диагностического поиска в начальной стадии болезни больные могут не предъявлять жалоб, и заболевание будет диагностировано на последующих этапах. Жалобы общего характера (слабость, потливость, нижение массы тела) могут быть при самых разных заболеваниях, ПОЭТОМУ рассматривать их на I этапе как специфические для ХМЛ нельзя. Лишь озже, при выявлении других симптомов, указывающих на ХМЛ, они мо-Ут быть интерпретированы как выражение миелопролиферативного син-
1яжесть и боли в области левого и правого подреберий обычно объяснится увеличением селезенки и печени. В сочетании с жалобами общего Pj*KTepa и болями в костях они могут ориентировать врача на миелопро-вдферативное заболевание.
В терминальной стадии болезни часть жалоб может быть обусловле возникновением осложнений: гнойно-воспалительных, геморрагически диатеза, мочекислого диатеза. г°
На I этапе можно получить сведения об изменениях гемограммы и гт водившемся ранее лечении (цитостатические препараты). Следовательн " если в поле зрения врача попадает больной, которому уже ставили диагн°" ХМЛ, последующий диагностический поиск значительно упрощается. Ва*3 но выяснить у больных сведения о проводившемся лечении и неэффектщГ ности препаратов, до данного момента улучшающих общее состояние сни" жавших количество лейкоцитов. Такая информация позволит предполо" жить переход в поликлоновую (терминальную) стадию болезни.
На II этапе диагностического поиска возможно получение сведений, позволяющих высказать предположение: 1) о характере патологического процесса, т.е. существе самого заболевания; 2) о стадии заболевания; 3) о возможных осложнениях.
В развернутой и терминальной стадиях выявляются признаки, в существенной мере подтверждающие предположение о ХМЛ: бледность кожных покровов (обусловлена нарастающей анемизацией), кожные геморрагии и инфильтраты (более характерны для терминальной стадии ХМЛ). Существенным признаком является спленомегалия (без увеличения лимфатических узлов), сочетающаяся с увеличением печени, что при соответствующих жалобах и анамнезе может быть расценено как проявление миелопро-лиферативного синдрома.
При развитии осложнений, например инфаркте селезенки, отмечается резкая болезненность ее при пальпации, шум трения брюшины над селезенкой. Постепенно селезенка становится плотной (ее масса составляет 6-9 кг, спускается нижним полюсом в малый таз).
Наиболее важные данные для диагноза ХМЛ получают на III этапе диагностического поиска.
В I стадии болезни в периферической крови выявляют лейкоцитоз (более 50 109/л с нейтрофилезом (гранулоциты всех стадий созревания - мие-лоциты, юные, палочкоядерные), эозинофильно-базофильную ассоциацию. Количество тромбоцитов не изменено (иногда немного увеличено). Иногда выявляется небольшое количество бластов - до 1-3 %. Костный мозг богат клеточными элементами с преобладанием элементов гранулоцитарного ряда. Количество эозинофилов, базофилов, гранулоцитов может быть увеличено.
Во II стадии количество лейкоцитов составляет 50-500 109/л, увеличено содержание незрелых форм (промиелоциты составляют 20-30 %), бласты составляют до 10 %, тромбоциты снижены или увеличены. В костном мозге отмечается выраженная многоклеточность, в лейкограмме сдвиг влево резко выражен, увеличено содержание промиелоцитов, бластов - около 10 %
В III стадии количество лейкоцитов невелико (до 50 109/л), много незрелых форм, бласты составляют более 10 %, среди них встречаются уродливые формы. Количество тромбоцитов снижено. В костном мозге содержание бластов увеличено, эритропоэз и тромбоцитопоэз угнетены.
Функциональные свойства лейкоцитов и содержание в них ферменто изменены: снижена активность щелочной фосфатазы нейтрофилов, наРув шена способность к фагоцитозу. При пункции увеличенной селезеНК|Уь1Х развернутой стадии болезни обнаруживается преобладание миелоид клеток (что в норме никогда не встречается). й.
Данный этап оказывается решающим в идентификации бластного Р _ за: нарастание количества бластных клеток в костном мозге и перифер
0й крови (суммарное количество бластов и промиелоцитов равно 20 % с1С?ллее тогда как вне бластного криза это количество обычно не превышает 10-15 %)-
Сиинтиграфия костей помогает обнаружить увеличение плацдарма кро-творения (исследование производят при неясном диагнозе; оно не являйся обязательным для всех больных ХМЛ).
Диагностика. Выявление ХМЛ в развернутой стадии болезни не пред-тавляет трудностей и основывается на характерных данных анализа крови, С ультатах исследования костного мозга, увеличении печени и селезенки. ^ Диагностическими критериями заболевания являются: . лейкоцитоз более 20-109/л;
Появление в лейкоцитарной формуле пролиферирующих форм (мие- лобласты и промиелоциты) и созревающих гранулоцитов (миелоциты, ме-
Тамиелоциты);
Миелоидная пролиферация костного мозга (по данным миелограммы
И трепанобиопсии);
Снижение активности щелочной фосфатазы нейтрофилов (менее
Обнаружение Ph-хромосомы в кроветворных клетках;
Расширение «плацдарма» кроветворения (по данным сцинтиграфии
Увеличение размеров селезенки и печени. Дифференциальная диагностика. ХМЛ следует дифференцировать от так
Называемых лейкемоидных реакций, которые могут возникать при ряде заболеваний (туберкулез, рак, различные инфекции, почечная недостаточность и пр.). По определению А.И. Воробьева, лейкемоидная реакция - это «изменения в крови и органах кроветворения, напоминающие лейкозы и другие опухоли кроветворной системы, но не трансформирующиеся в ту опухоль, на которую они похожи». При лейкемоиднои реакции наблюдается высокий лейкоцитоз, в периферической крови появляются незрелые нейтрофилы, однако базофильно-эозинофильная ассоциация не обнаруживается. Дифференциальный диагноз основывается на выявлении основного заболевания (рак, туберкулез и пр.), а также на повышении активности щелочной фосфатазы нейтрофилов (вместо ее снижения при ХМЛ). При стернальной пункции для лейкемоиднои реакции характерно увеличение содержания миелоцитов, однако Ph-хромосома никогда не обнаруживается.
Лечение. Основная задача лечения любого гемобластоза (в том числе и ХМЛ) - ликвидация или подавление роста патологического клона клеток. Однако применительно к хроническим лейкозам это не означает, что любого больного, у которого обнаруживается заболевание системы крови, сразу же нужно активно лечить цитостатическими препаратами, подавляющими опухолевый рост.
В начальной стадии болезни (при хорошем самочувствии, но несо мненных изменениях в периферической крови и костном мозге) необходи мы общеукрепляющая терапия, правильное питание, соблюдение режима
РУда и отдыха (очень важно избегать инсоляции). Больной должен находиться под наблюдением врача; периодически (1 раз в 3-6 мес) необходимо исследовать периферическую кровь.
При появлении симптомов прогрессирования болезни необходимо Роводить цитостатическую терапию, при этом объем такого лечения зави- ит от стадии заболевания. При появлении отчетливых симптомов опухо- евого роста (увеличение размеров селезенки, печени, а также повышение
Количества лейкоцитов по сравнению с предшествующим периодом бот ни) проводят так называемую первично-сдерживающую терапию. Обыч^ лечение начинают при содержании лейкоцитов 50-70-109/л. Амбулатоп ° применяют гидроксимочевину (гидреа) в невысоких дозах (при обязател ном гематологическом контроле); после достижения клинической и/и гематологической ремиссии решается вопрос о поддерживающей терапии
В развернутой стадии болезни объем химиотерапии зависит «группы риска», определяемой наличием неблагоприятных признаков- °Т
1) лейкоцитоз более 200109/л, бластов более 3 %, сумма бластов и пп0 миелоцитов в крови более 20 %, количество базофилов в крови более 10%"¦
2) снижение гемоглобина до уровня менее 90 г/л;
3) тромбоцитоз более 500 109/л или тромбоцитопения менее 100 109/л-
4) спленомегалия (селезенка пальпируется на 10 см ниже реберной дуги и более);
5) гепатомегалия (печень пальпируется на 5 см ниже реберной дуги и более).
Низкий риск - наличие одного признака; промежуточный риск - наличие 2-3 признаков; высокий риск - наличие 4 признаков и более. При низком и промежуточном риске изначально показана монохимиотерапия при высоком риске с самого начала рекомендуется полихимиотерапия.
В развернутой стадии проводится курсовая химиотерапия. Используют гидреа, но в больших дозах (ежедневно 2-3 приема) под гематологическим контролем: при снижении количества лейкоцитов и тромбоцитов дозу препарата уменьшают, а при содержании лейкоцитов 10-20 109/л и тромбоцитов 100-109/л препарат отменяют. Если ранее эффективные препараты не оказывают действия в течение 3-4 нед, то следует провести курс лечения другим цитостатиком. Так, если гидреа оказывается неэффективной, то назначают миелосан (бусульфан, милеран), миелобромол.
После курсовой химиотерапии проводится поддерживающая терапия по схеме, близкой к схеме первично-сдерживающей терапии. Применяют препараты, оказавшие терапевтический эффект при курсовой химиотерапии.
Полихимиотерапия проводится курсами при высокой степени риска, а также в терминальной стадии ХМЛ; при бластном кризе - в объеме, соответствующем терапии при ОЛ. Используют препараты, оказывающие ци-тостатическое действие на пролиферирующие элементы (цитозар, мето-трексат, винкристин, противоопухолевый антибиотик рубомицина гидрохлорид). Курсы полихимиотерапии короткие (5-14 дней с перерывами в 7-10 дней).
В настоящее время появились принципиально новые методы лече ния ХМЛ - цитокин а-интерферон (а-ИФН). Дело в том, что в процессе миелоидной пролиферации мегакариоциты и тромбоциты выделяют боль шое количество ростовых факторов, которые сами по себе способствуют дальнейшей пролиферации мутантных полипотентных и олигопотентны стволовых клеток, а кроме того, и стромальных клеток. Все это ведет дальнейшему прогрессированию болезни, а также развитию фиброзных и менений в костном мозге. Между тем доказано, что а-ИФН по своему хи мическому строению и функциональным свойствам является антагонист ростовых факторов; он выделяет субстанции, которые тормозят стимул рующее действие мегакариоцитов на кроветворение и обладают антипро- феративной активностью по отношению к родоначальным клеткам кро ^ творения; кроме того, а-ИФН стимулирует противоопухолевый иммунй ^ Следовательно, создаются условия для сохранения нормального крове
Ия, при этом а-ИФН не обладает цитостатическим действием, что яв-РеНтсЯ" весьма привлекательным свойством, так как отсутствует депрессив-лЯе влияние на нормальные клетки костного мозга. Н° На практике используют рекомбинантный а-ИФН - реаферон, или
Тпон «А», который вводится внутримышечно или подкожно в дозах йН 2 до 9 МИ/м2 в день (по данным разных авторов) в течение 2-6 мес /f МИ = 1 °00 °°0 ЕД)" позволяющий добиться гематологической ремис-
И v многих больных. При лечении этим препаратом возможно появление "типпоподобного» синдрома - повышение температуры, головная боль, "омота в мышцах, общее плохое самочувствие, однако прием парацетамола ^пирует эти явления.
Интрон «А» иногда комбинируют с цитостатическим препаратом - гидреа или цитозин-арабинозидом (цитозаром), что позволяет улучшить пезультаты лечения; 5-летняя выживаемость при лечении интроном «А» 32-89 мес (у 50 % больных), тогда как при лечении миелосаном этот показатель равен 44-48 мес.
Весьма существенно, что при лечении а-ИФН может наступить не только гематологическая, но и цитогенетическая ремиссия, когда в клетках крови и костного мозга Ph-хромосома вообще не определяется, что позволяет говорить не столько о ремиссии, сколько о полном выздоровлении от
В настоящее время основным «событием» в лечении ХМЛ является новый препарат - блокатор мутантной тирозинкиназы (белок р210) - гливек (STI-571). Препарат назначают в дозе 400 мг/м2 в течение 28 дней. При бластном кризе ХМЛ доза составляет 600 мг/(м2-сут). Применение препарата приводит к полной ремиссии заболевания без эрадикации опухолевого клона. В настоящее время гливек является препаратом выбора при ХМЛ.
При значительном увеличении селезенки иногда осуществляют облучение рентгеновскими лучами, что приводит к уменьшению ее размеров.
При гнойно-воспалительных осложнениях проводят антибиотикоте-рапию.
Гемотрансфузии при ХМЛ показаны при выраженном анемическом синдроме, не поддающемся цитостатической терапии, или лечении препаратами железа при железодефицитном ее происхождении. Больных ХМЛ ставят на диспансерный учет, проводят периодические осмотры с обязательным гематологическим контролем.
Прогноз. Длительность жизни больных ХМЛ в среднем составляет 3-5 лет, у некоторых больных достигает 7-8 лет. Продолжительность жизни после бластного криза редко превышает 12 мес. Использование интрана А существенно изменяет прогноз заболевания к лучшему.
Профилактика. Мер предупреждения ХМЛ не существует, в связи с чем можно говорить лишь о вторичной профилактике болезни, которая состоит в предупреждении обострений болезни (поддерживающая терапия, исключение инсоляции, простудных заболеваний и пр.).
Эритремия (истинная полицитемия, болезнь Вакеза)
Эритремия (ЭР) является миелопролиферативным заболеванием, хро-
Ическим, доброкачественно текущим лейкозом, при котором наблюдается
Овышенное образование эритроцитов, а также нейтрофильных лейкоци-
Ов и тромбоцитов. Источник опухолевого роста - клетка-предшественни-
Ца миелопоэза.
Заболеваемость эритремиеи составляет около 0,6 на 10 000 населения. Одинаково часто болеют как мужчины, так и женщины. Эритремия является болезнью лиц пожилого возраста: средний возраст заболевших 55-60 лет, однако заболевание возможно в любом возрасте.
Этиология. Причины развития заболевания неизвестны.
Патогенез. В основе эритремии лежит опухолевая клональная пролиферация всех трех ростков кроветворения - красного, гранулоцитарного и мегакариоцитарного, однако доминирует рост красного ростка. В связи с этим основным субстратом опухоли являются созревающие в избыточном количестве эритроциты. Появляются очаги миелоидного кроветворения в селезенке и печени (чего никогда не бывает в норме). Увеличенное количество эритроцитов и тромбоцитов в периферической крови снижает скорость кровотока, повышает вязкость и свертываемость крови, что обусловливает появление ряда клинических симптомов.
Классификация. Учитывают стадию течения болезни, вовлечение в патологический процесс селезенки и последующую трансформацию эритремии в другие заболевания системы крови.
Стадия I - начальная: содержание гемоглобина на верхней границе нормы, небольшое увеличение массы циркулирующих эритроцитов, селезенка увеличена незначительно (за счет переполнения кровью) или без изменений. АД нормальное или слегка повышено, отмечается очаговая гиперплазия костного мозга в трепанате из подвздошной кости. Продолжительность I стадии может превышать 5 лет.
Стадия II - развернутая: фаза А - без миелоидной метаплазии селезенки (простой вариант плеторы без спленомегалии). Тотальная трехро-стковая гиперплазия костного мозга. Отсутствие экстрамедуллярного гемо-поэза; фаза Б - с миелоидной метаплазией селезенки. Большой миелопро-лиферативный синдром: панцитоз в периферической крови, в костном мозге имеется панмиелоз с очаговым миелофиброзом или без него, миело-идная метаплазия селезенки с фиброзом или без него.
Стадия III - терминальная: перерождение доброкачественной опухоли в злокачественную (миелофиброз с анемизацией, хронический миело-лейкоз, острый лейкоз). Миелофиброз развивается практически у всех болеющих более 10-15 лет; он отражает естественную эволюцию болезни. Признаком миелофиброза является цитопения (анемия, тромбоцитопения, реже - лейкопения). Развитие хронического миелолейкоза проявляется на^ растанием лейкоцитоза, увеличением (или появлением) в периферической крови миелоцитов, промиелоцитов, а также обнаружением в клетках крови и костного мозга Ph-хромосомы.
Острый лейкоз развивается обычно у больных, леченных цитостатика-ми и радиоактивным фосфором.
Анемия у больных эритремиеи может быть связана с частыми кровопусканиями, повышенным депонированием эритроцитов, а также их гемолизом.
Клиническая картина. Эритремия проявляется двумя большими синдромами.
Плеторический синдром обусловлен увеличенным содержанием эритроцитов, а также лейкоцитов и тромбоцитов (плетора - полнокровие). Этот синдром обусловлен: 1) появлением субъективных симптомов; 2) нарушениями сердечно-сосудистой системы; 3) изменениями лабораторных показателей.
1. К субъективным симптомам плеторического синдрома относятся головные боли, головокружения, ухудшение зрения, стенокардия, кожный зуд, эритромелалгия (внезапное возникновение гиперемии с си-
Нюшным оттенком кожи пальцев рук, сопровождающееся резкими болями и жжением), возможны ощущения онемения и зябкости конечностей.
2. Нарушения сердечно-сосудистой системы проявляются в изменении окраски кожных покровов и видимых слизистых оболочек по типу эритро-ццаноза, особенности окраски слизистой оболочки в месте перехода мягкого неба в твердое (симптом Купермана), АГ, развитии тромбоза, реже кровоточивости. Помимо тромбозов, возможны отеки голеней и эритромелалгия. Нарушения кровообращения в артериальной системе могут приводить к тяжелым осложнениям: острому инфаркту миокарда, инсультам, нарушению зрения, тромбозу почечных артерий.
3. Изменения лабораторных показателей: увеличение содержания гемоглобина и эритроцитов, повышение показателей гематокри-Та и вязкости крови, умеренный лейкоцитоз со сдвигом лейкоцитарной формулы влево, тромбоцитоз, резкое замедление СОЭ.
Миелопролиферативный синдром обусловлен гиперплазией всех трех ростков кроветворения в костном мозге и экстрамедуллярно. Он включает: 1) субъективные симптомы, 2) спленомегалию и(или) гепатомегалию, 3) изменения лабораторных показателей.
1. Субъективные симптомы: слабость, потливость, повышение темпера туры тела, боли в костях, тяжесть или боль в левом подреберье (вследствие
Спленомегалии).
2. Спленомегалия объясняется не только миелоидной метаплазией органа (появление очагов экстрамедуллярного кроветворения), но и застоем крови. Реже наблюдается увеличение печени.
3. Среди лабораторных показателей наибольшее диагностическое значение имеют отклонения от физиологической нормы в периферической крови: панцитоз, чаще со сдвигом лейкоцитарной формулы влево; при трепа-нобиопсии выявляется трехростковая гиперплазия костного мозга, в пунк-тате селезенки - очаги миелоидной метаплазии органа.
Различная выраженность синдромов на разных стадиях болезни обусловливает чрезвычайную вариабельность клинической картины. Можно наблюдать больных с несомненной эритремиеи, почти не предъявляющих жалоб и полностью трудоспособных, и больных с тяжелым поражением внутренних органов, нуждающихся в проведении терапии и утративших трудоспособность.
На I этапе диагностического поиска в начальной стадии заболевания больные могут не предъявлять никаких жалоб. По мере прогрессирования болезни жалобы связаны с наличием и выраженностью плеторы и миело-пролиферативного процесса. Наиболее часты жалобы «плеторического» характера, обусловленные повышенным кровенаполнением сосудов и функциональными нейрососудистыми расстройствами (головные боли, эритромелалгия, нарушение зрения и пр.). Вся эта симптоматика может быть связана и с другими заболеваниями, что необходимо выяснить при Дальнейшем обследовании больного.
Жалобы, обусловленные наличием миелопролиферативного синдрома (потливость, тяжесть в левом подреберье, боли в костях, повышение температуры тела) также неспецифичны для эритремии. Достаточно характерен кожный зуд, который появляется после приема водных процедур. Этот симптом наблюдается у 55 % больных в развернутой стадии и объясняется гиперпродукцией базофилов и гистаминемией. Аналогична природа крапивницы, наблюдающейся у 5-7 % больных.
Перечисленные симптомы имеют значение для определения стадии эритремии: обычно они свидетельствуют о переходе болезни в развернутую
Или терминальную стадию с развитием миелофиброза как наиболее частого исхода эритремии.
В анамнезе больных могут быть такие осложнения заболевания, как инсульты, инфаркты миокарда. Иногда болезнь дебютирует именно этими осложнениями, а истинная причина их развития - эритремия - выявляется при обследовании больного по поводу инсульта или инфаркта миокарда
Указания на проводимое ранее лечение радиоактивным фосфором, ци-тостатиками или кровопусканиями могут навести на мысль о наличии какого-либо опухолевого заболевания крови. Уменьшение симптоматики плеторического синдрома на фоне лечения указанными средствами позволяет предположить эритремию.
На II этапе диагностического поиска можно выявить отчетливые симптомы лишь во II (развернутой) стадии болезни. Обнаруживают в основном признаки плеторического синдрома: эритроцианоз, инъецированные сосуды конъюнктивы («кроличьи глаза»), отчетливая цветовая граница в месте перехода твердого неба в мягкое. Можно выявить симптомы эритро-мелалгии: отек кончиков пальцев, стоп, нижней трети голени, сопровождающийся локальной гиперемией и резким жжением.
При исследовании сердечно-сосудистой системы диагностируют АГ и увеличение левого желудочка, в развернутой стадии болезни - «пестрые ноги» (изменение окраски кожных покровов голеней, преимущественно дистальной их части) в виде участков пигментации различной интенсивности, обусловленных нарушением венозного кровообращения.
При пальпации живота можно обнаружить увеличение селезенки, что является одним из характерных признаков болезни. Увеличение селезенки может быть обусловлено: 1) повышенным депонированием элементов крови; 2) «рабочей» гипертрофией вследствие увеличения ее секвестрирующей функции; 3) экстрамедуллярным кроветворением (миелоидная метаплазия с преобладанием эритропоэза). Эти причины часто сочетаются. Увеличение печени обусловлено аналогичными причинами, а также развитием фиброза и неспецифического реактивного гепатита. Следует иметь в виду, что гепа-томегалия может наблюдаться при злокачественной опухоли печени с развитием вторичного эритроцитоза.
Осложнения эритремии в виде тромбозов сосудов головного мозга выражаются рядом очаговых симптомов, выявляемых при исследовании
Однако и на II этапе поставить окончательно диагноз эритремии нельзя, так как многие ее симптомы могут быть при симптоматических эритро-цитозах. Кроме того, такие симптомы, как АГ, спленомегалия и гепатоме-галия, характерны для самых разнообразных заболеваний.
В связи с этим III этап диагностического поиска приобретает решающее значение, так как позволяет: а) поставить окончательный диагноз; б) уточнить стадию эритремии; в) выявить осложнения; г) осуществить контроль за лечением.
Анализ периферической крови обнаруживает эритроцитоз, увеличение содержания гемоглобина и показателя гематокрита, что, однако, встречается и при симптоматических эритроцитозах. Диагностическое значение имеет повышение уровня гемоглобина в сочетании с эритроцитозом, лейкоцитозом и тромбоцитозом. При исследовании лейкоцитарной формулы обнаруживают сдвиг влево до незрелых форм гранулоцитов. Если изменения в периферической крови незначительны или данные неубедительны (например, эритроцитоз не сочетается с тромбоцитозом), то необходимо провести исследование костного мозга (трепанобиопсия). Наличие в трепанате тоталь-442
Лой трехростковой гиперплазии костного мозга с преобладанием формен-Hbix элементов эритропоэза, замещение жировой ткани красным ростком костного мозга дают возможность поставить окончательный диагноз. Расширение «плацдарма» кроветворения выявляется также с помощью радио-нуклидного сканирования костей с 32Р. Гистохимическое исследование выявляет повышенную активность щелочной фосфатазы нейтрофилов.
Осложнения. Течение эритремии осложняют: 1) сосудистые тромбозы (мозговых, коронарных, периферических артерий); 2) геморрагический синдром: кровотечения после малых оперативных вмешательств (экстракция зуба), из сосудов пищеварительного тракта, геморроидальных узлов, что обусловлено плохой ретракцией кровяного сгустка вследствие изменения функциональных свойств тромбоцитов; 3) эндогенная урикемия и ури-козурия (вследствие повышенной гибели клеток на ядерных предстадиях их созревания), что проявляется симптомами мочекаменной болезни и подагрического артрита.
Исходами болезни являются ситуации, указанные в III стадии течения болезни (миелофиброз, хронический миелолейкоз, острый лейкоз, анемия).
Диагностика. Эритремию можно заподозрить у лиц с наличием стойкого эритроцитоза в сочетании с нейтрофильным лейкоцитозом, тромбоцитозом при отсутствии заболеваний (или состояний), которые могли бы вызвать эритроцитоз.
Диагностическими критериями эритремии (в развернутой стадии) являются:
Увеличение массы циркулирующих эритроцитов.
Нормальное насыщение артериальной крови кислородом (более 92%).
Лейкоцитоз более 12 109/л (при отсутствии явных причин для появления лейкоцитоза).
Тромбоцитоз более 400-109/л.
Увеличение содержания щелочной фосфатазы нейтрофилов (при отсутствии инфекции).
Увеличение ненасыщенной витамин В12-связывающей способности сыворотки крови.
Диагноз ЭР достоверен при наличии трех признаков категории А или Двух признаков категории А и одного признака категории Б.
Затруднения в постановке диагноза обусловлены развитием так называемого симптоматического эритроцитоза при целом ряде заболеваний. Выделяют абсолютные и относительные эритроцитозы. При абсолютных эритроцитозах отмечают увеличение массы циркулирующих эритроцитов и повышенный эритропоэз. Для относительных эритроцитозов характерны уменьшение объема циркулирующей плазмы и нормальная масса циркулирующих эритроцитов. Относительные эритроцитозы часто выявляют у мужчин, страдающих гипертонией, ожирением, неврастенией, принимающих мочегонные средства. Вторичный абсолютный эритроцитоз развивается у курящих, он обусловлен увеличением содержания в крови окиси углерода.
Причины развития симптоматических эритроцитозов: 1) генерализованная тканевая гипоксия (легочная патология, заболевания сердца, гемоглобинопатии, ожирение и т.д.); 2) паранеопластические реакции (опухоли Ночек, опухоли коркового и мозгового вещества надпочечников, гипофиза, яичников, сосудистые опухоли, опухоли других органов); 3) ишемия почек
(стеноз почечной артерии, гидронефроз, поликистоз и другие аномалии почек); 4) неустановленные причины (заболевание ЦНС, портальная ги-пертензия).
Относительные эритроцитозы наблюдаются при эксикозах (обезвоживание вследствие поноса, рвоты, повышенной потливости и др.). Дифференциальная диагностика основывается на учете всей клинической картины. В сложных случаях необходимо исследовать содержание эритропоэти-на в крови; при эритремии оно не повышается.
Формулировка развернутого клинического диагноза включает сведения о-1) стадии заболевания; 2) наличии осложнений; 3) фазе процесса (обострение или ремиссия); 4) наличии выраженных синдромов (портальная гипер-тензия, АГ и пр.).
Лечение. Весь комплекс лечебных мероприятий при ЭР представляется следующим.
В развернутой стадии болезни при наличии плеторического синдрома, но без лейко- и тромбоцитоза применяют кровопускания как самостоятельный метод терапии, при этом необходимо добиваться снижения уровня гематокрита до нормальных значений (менее 45 %). Забирают по 400-500 мл крови через день (в условиях стационара) или через 2 дня (в условиях поликлиники). Для профилактики тромбозов (развиваются в результате кровопускания, а также как осложнение эритремии) назначают ацетилсалициловую кислоту в дозе 0,5-1 г/сут накануне и в день кровопускания, а затем в течение 1-2 нед после окончания кровопусканий. Кроме ацетилсалициловой кислоты, назначают и другие дезагреган-ты - тиклид, плавике, пентоксифиллин. Перед кровопусканием для профилактики тромбоэмболии легочной артерии целесообразно вводить внутривенно 5000 ЕД гепарина (через иглу Дюфо), а также по 5000 ЕД гепарина под кожу живота 2 раза в сутки в течение нескольких дней после кровопускания. При плохой переносимости кровопусканий, наблюдаемой у лиц с выраженным атеросклерозом мозговых сосудов, ограничиваются эксфу-зией 350 мл (2 раза в неделю). При кровопусканиях необходимо снизить гемоглобин до 150 г/л.
Если кровопускания недостаточно эффективны, а также при формах болезни, протекающих с панцитозом и спленомегалией, назначают цито-статическую терапию. Возраст больных более 55 лет расширяет показания к применению цитостатиков. Косвенными показаниями к цитостатической терапии являются и другие признаки миелопролиферативного синдрома (зуд), а также тяжесть заболевания, висцеральные сосудистые осложнения (инсульт, инфаркт миокарда), истощение.
Противопоказания к цитостатической терапии: молодой возраст больных, рефрактерность к лечению на предыдущих этапах, а также чрезмерно активная в прошлом цитостатическая терапия из-за опасения перехода заболевания в фазу анемии. Эффект цитостатической терапии следует оценивать через 3 мес после окончания лечения; это объясняется тем, что продуцированные до лечения эритроциты живут в среднем около 2-3 мес. Снижение количества лейкоцитов и тромбоцитов наступает значительно раньше, соответственно срокам их жизни. Критерием эффективности цитостатической терапии является достижение гематологической ремиссии (полной, когда все показатели крови нормализуются, или частичной, при которой остается несколько повышенным количество эритроцитов, лейкоцитов и/или тромбоцитов).
Из цитостатических препаратов на первом этапе обычно назначают гидроксимочевину (гидреа) в дозе 30-50 мг/(кгсут) (по 2-3 капсулы в
День). Во время лечения необходимо контролировать число лейкоцитов. Гидреа сочетают с а-интерфероном в дозе 3-5 млн ME подкожно 3-7 раз в неделю длительно (не менее года), что позволяет купировать тромбоци-тоз, плетору, кожный зуд.
При гипертромбоцитозе применяют анагрелид.
На исходы эритремии (миелофиброз, острый лейкоз, хронический миелолейкоз) воздействуют согласно принципам лечения этих заболеваний: при миелофиброзе применяют анаболические стероиды, нитостати-ки и переливания эритроцитной массы; при остром лейкозе показана полихимиотерапия, при хроническом миелолейкозе - цитостатические препараты.
Симптоматическую терапию при приступах эритромелалгии проводят с помощью антиагрегантов, нестероидных противовоспалительных препаратов (ацетилсалициловая кислота, индометацин). Артериальную гипертонию, приступы стенокардии ликвидируют в соответствии с правилами лечения этих состояний.
При осложнениях эритремии тромбозом сосудов применяют анти-коагулянтную и антиагрегантную терапию.
Больных эритремией ставят на диспансерный учет с частотой обращения к врачу и назначением анализов периферической крови 1 раз в 3 мес.
Прогноз. При неосложненном течении эритремии продолжительность жизни может достигать 15-20 лет (в дальнейшем возникают осложнения). Если же осложнения со стороны сердечно-сосудистой системы развиваются достаточно рано или болезнь прогрессирует, продолжительность жизни сокращается. Своевременно начатая терапия удлиняет продолжительность жизни, хотя это наблюдается не во всех случаях.
Профилактика. Радикальных мер предупреждения болезни не существует, в связи с чем можно говорить лишь о вторичной профилактике, заключающейся в динамическом наблюдении за больными и проведении проти-ворецидивной терапии.
Клинигеский анализ крови при хроническом миелолейкозе . В периферической крови на момент диагностики выявляется лейкоцитоз, обычно более 50 10 9 /л (возможен и более низкий уровень лейкоцитов - 15-20 109/л) со сдвигом влево за счет палочкоядерных нейтрофилов, метамиелоцитов, миелоцитов, редко - промиелоцитов.
Могут выявляться единичные бластные клетки (прогностически неблагоприятный признак). Характерна эозинофильно-базофильная ассоциация - увеличение количества эозинофилов и базофилов, часто морфологически аномальных. В 30% случаев определяется нормохромная нормоцитарная анемия легкой степени, у 30% больных выявляется тромбоцитоз; реже - тромбоцитопения (неблагоприятный признак).
Миелограмма при
. При исследовании миелограммы (которая не всегда необходима для постановки диагноза) выявляются гиперклеточный костный мозг и гиперплазия нейтрофильного ростка (лейкоэритробластическое соотношение достигает 10-20:1 и более). Гранулоциты при хроническом миелолейкозе обладают практически нормальной фагоцитарной и бактерицидной активностью.
Количество клеток базофильного и эозинофильного рядов
увеличено, нередко встречаются аномальные формы; возможен мегакариоцитоз.
Гистологигеское исследование костного мозга при хроническом миелолейкозе . При исследовании костного мозга методом трепанобиопсии выявляется его гиперклеточность и выраженная миелоидная гиперплазия (лейко-эритробластическое соотношение более 10:1); количество предшественников эритроцитов уменьшено. Мегакариоцитоз отмечается у 40-50%, возможен морфологический атипизм клеток. При прогрессировании (фаза акселерации) нередко развивается ретикулиновый, реже - коллагеновый фиброз костного мозга.
Цитогенетическое и молекулярно-генетическое исследование при хроническом миелолейкозе . При цитогенетическом исследовании у 95-97% больных выявляется Ph-хромосома. При отсутствии Ph-хромосомы методом флюоресцентной гибридизации in situ (FISH) можно обнаружить 1 клетку с транслокацией BCR-ABL на 200-500 нормальных клеток. Метод удобен для мониторинга минимальной остаточной болезни, выполняется на образцах периферической крови, цитологических и морфологических препаратах крови и костного мозга, срезах гистологических препаратов.
Для диагностики и мониторирования заболевания используется также ПЦР, которая позволяет выявить одну патологическую клетку среди 10 4 -10 6 нормальных.
При отрицательных результатах обоих методов (цитогенетического и молекулярно-генетического) диагностируется один из вариантов МДС/МПЗ.
При молекулярно-генетических исследованиях у больных в фазе акселерации и бластном кризе выявляются повреждения ряда генов (ТР53, RBI, MYC, RAS, pl6, AML1, EVI1), однако их роль в трансформации заболевания пока не установлена.

Цитохимические исследования при хроническом миелолейкозе . Характерным цитохимическим признаком развернутой фазы хронического миелолейкоза является резкое снижение уровня щелочной фосфатазы нейтрофилов - до 2-4 ед. (норма - 8-80 ед.). Нормальные или повышенные показатели не исключают диагноза хронического миелолейкоза.
Биохимические исследования при хроническом миелолейкозе . Характерно увеличение уровня сывороточного витамина В12 и витамин В12-связывающей способности сыворотки крови вследствие увеличенной продукции транскобаламина гранулоцитами. Повышенное разрушение клеток приводит к гиперурикемии, особенно при цитостатической терапии. Может выявляться также повышение железосвязывающей способности сыворотки крови, уровня гистамина, снижение лейцинаминопептидазы.
Диагноз хронического миелолейкоза ставится на основании клинико-лабораторных данных (спленомегалия, лейкоцитоз со сдвигом в лейкоцитарной формуле влево и наличием промежуточных форм нейтрофилов, эозинофильно-базофильная ассоциация, усиленный миелопоэз в костном мозге, низкий уровень щелочной фосфатазы нейтрофилов) и подтверждается обнаружением Ph-хромосомы, t(9;22)(q34;qll.2) или гена BCR-ABL (цитогенетическими или молекулярно-генетическими методами).
Выделяют 3 стадии хронического миелолейкоза : хроническую, фазу акселерации и бластный криз.

Критерии для определения стадии хронического миелолейкоза (ВОЗ)
Хроническая фаза хронического миелолейкоза: нет признаков других фаз заболевания; нет симптомов (после лечения).
Фаза акселерации (при наличии одного и более признаков) хронического миелолейкоза:
1) 10-19% бластов в крови или костном мозге;
2) количество базофилов в периферической крови не менее 20%;
3) персистирующая тромбоцитопения (меньше 100 10 9 /л), не связанная с лечением, или персистирующий тромбоцитоз больше 1000 10 9 /л, резистентный к терапии;
4) нарастающие спленомегалия и лейкоцитоз, резистентные к терапии (удвоение количества лейкоцитов меньше 5 дней);
5) новые хромосомные изменения (появление нового клона).
Наряду с одним из вышеперечисленных признаков фазы акселерации обычно выявляется пролиферация мегакариоцитов, ассоциирующаяся с ретикулиновым или коллагеновым фиброзом, или выраженная дисплазия гранулоцитарного ростка.
Бластный криз хронического миелолейкоза:
1) не менее 20% бластов в крови или костном мозге;
2) экстрамедуллярная пролиферация властных клеток;
3) большое количество агрегатов бластных клеток в трепанобиоптате.
Основной лабораторный признак фазы акселерации и бластного криза - прогрессирующее увеличение промиелоцитов и бластов в периферической крови и костном мозге. При цитохимических исследованиях в фазе бластного криза у 70% пациентов определяется миелоидный, у 30% - лимфоидный вариант, которые имеют сходные черты соответственно с ОМЛ и ОЛЛ:
а) средний возраст больных с лимфоидным кризом меньше, чем больных с миелоидным;
б) нейролейкоз чаще развивается у больных с лимфоидным кризом;
в) непосредственные результаты лечения при лимфоидном варианте криза существенно лучше.